作者:上海太阳能工程技术研究中心有限公司 硅材料研究室经理 张愿成
上海太阳能工程技术研究中心有限公司 副总经理 张滢清
随着光伏发电产业的发展,多晶硅材料的需求加大。国内目前主要采用传统的西门子法或改良西门子法生产多晶硅。该方法生产多晶硅,每公斤太阳能级多晶硅将产生10~15公斤的SiCl4[1],如何处理高污染的SiCl4成为多晶硅生产厂家面临的一个难题。针对这一难题,日本的新太阳硅公司,我国的锦州新世纪石英玻璃公司、上海电力学院太阳能研究所[2]及北京京仪世纪自动化设备有限公司先后提出了Zn还原法处理SiCl4同时制备多晶硅的工艺。Zn还原法具有工艺简短、反应速度快、产品质量稳定、低污染等优点。其主要反应原理为:
SiCl4(g) + 2Zn(g)→Si(s) + 2ZnCl2(g)
然而这种方法,按照反应式来计算,每制备一倍量的硅,就会产生十倍量的ZnCl2副产物,如何经济地有效回收利用ZnCl2,进一步降低生产成本本和污染成为一个重要问题。
金属氯化物的熔盐电解是生产镁和很多稀土金属的主要方法。与水电解相比,熔盐电解具有过电压小,产量高的优点[3]。Zn还原法的副产物中ZnCl2纯度较高,除少量的剩余反应物Zn之外,无其他杂质,不需要提纯处理,因此比较适合采用熔盐电解法进行电解。
另外,有专利和文献报道了在ZnCl2熔盐中加入KCl、NaCl等其他金属氯化物作为辅助电解质以提高电导率的工艺和方法[4-6]。然而,如利用Zn还原法制备太阳能级多晶硅,产品纯度要保证在99.9999%以上,这就要求整个闭环工艺中杂质含量越低越好,电解中应尽量避免引入其他金属杂质的机会。因此,本文探索了一种在不添加辅助电解质情况下,ZnCl2熔盐的电解工艺,并初步研究了电解电流,电解温度对槽电压的影响。
实验方法
原料准备
为验证不添加辅助电解质ZnCl2熔盐电解的可行性,选用了市售分析纯ZnCl2(含量>98%)作为实验原料。
电解槽结构设计
因为在高温,金属氯化物熔盐的腐蚀性大,电解所产生气体(如氯气等)的反应强烈,因而设备材料方面出现的问题较多。针对ZnCl2熔盐电解,以及低杂质源的要求,目前可行的方法是以石英材料作为电解槽的材料。
在熔盐电解中,为使电解质保持在电解温度,需要大量的热量。补充热量的方法有内热法和外热法两种。内热法是利用电解质的电阻所产生的热,而外热法是从电解槽外部用燃料等进行加热。根据实验条件,本文ZnCl2熔盐电解采用的是外热法进行加热。电解槽详细结构如图1所示。
[page]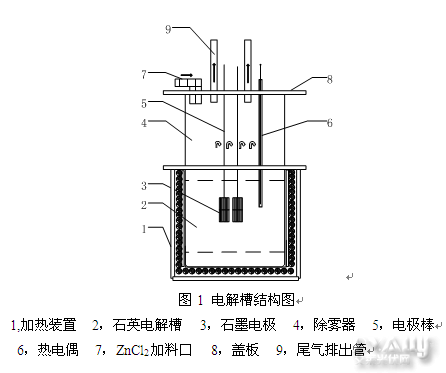
除湿工艺
ZnCl2易吸水,ZnCl2存放时以及在将ZnCl2置入电解槽的过程中会吸收水分。因此在电解前需将ZnCl2在250℃恒温加热24小时以上,除去ZnCl2中的水分,确保熔盐电解顺利进行。
电解实验
除湿以后,将电解槽升温至400℃以上,使ZnCl2完全熔融,然后控制工艺温度和电解电流,给电极供电,开始电解,并测量槽电压的值。实验过程中采用竖直式电极,生成的氯气可顺利向上排出,不与电解生成的Zn形成二次反应。产物Zn由于密度比ZnCl2大,从电极上滴落并汇集于底部,待电解结束后取出检测其纯度。另外,由于ZnCl2沸点较低,400℃以上的挥发性很大,实验装置中设置了一定高度的除雾器,ZnCl2挥发经除雾器自然冷却可落回电解槽中,这样即减少了原料损失,同时又避免了ZnCl2粉末堵塞出气管道。实验产生的尾气由排出管通入到吸收装置中。
结果与讨论
不同温度下槽电压与电流密度关系
将实验测得的不同温度下槽电压随电流密度变化的数据绘成曲线如图2,从图中可以看到,槽电压与电流密度在各温度下均呈线性关系。
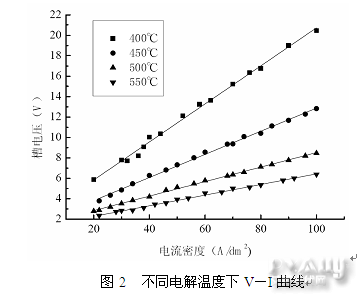
图2中各直线的斜率参见表1。槽电压均随电流密度的增加而增加,但在400℃和450℃条件下直线斜率相对较大,分别为0.186和0.113,槽电压随电流密度的增加上升较快。而在500℃和550℃条件下直线斜率相对较小,分别为0.071和0.052,槽电压上升缓慢。这应该是由于温度升高引起ZnCl2熔盐电导率上升,电阻降低造成的。
通过进一步研究槽电压与温度的关系,以及ZnCl2蒸汽压与温度的关系后,可以确定最佳的电解温度。[page]
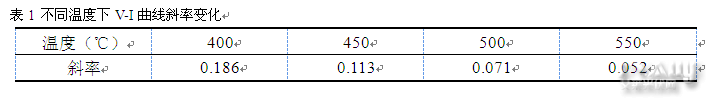
恒定电解电流下,槽电压与温度关系
将电流密度为50A/dm2下的槽电压随电解电流变化的数据绘制曲线如图2,此温度范围内两者近似表现为反比例递减关系。
由于ZnCl2电导率很低,仅为0.0024Ω-1ocm-1,熔盐电解的槽电压大小将主要由ZnCl2电解质的电阻和电极的极化决定。由于实验在比较小的电流密度下进行,可忽略阳极效应[3],熔盐电导率与槽电压可近似表现为下式中的反比关系:
λ=C/U (1)
λ:熔盐电导率,U:槽电压, C:常数
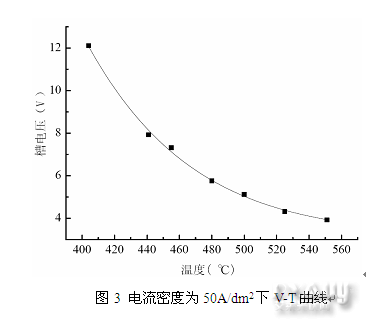
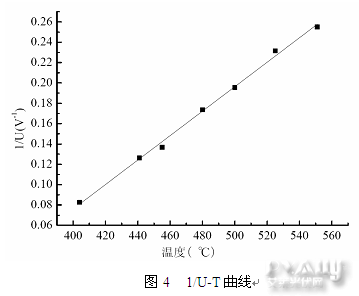
所以将图3改绘成如图4的1/U值与温度的曲线,即可反映ZnCl2熔盐电导率随温度的变化关系,温度越高,熔盐电导率就越高,其中550℃温度下的电导率是405℃时的3倍多。
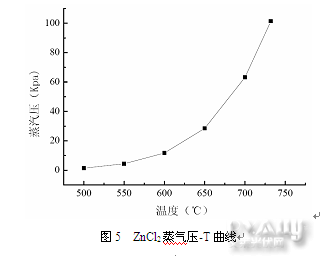
但是根据Clapeyron方程进行计算ZnCl2在不同温度下的蒸汽压结果,如图5所示。由于ZnCl2的挥发性很强,当温度升高,ZnCl2的蒸气压快速上升。从500℃上升到700℃,ZnCl2蒸气压迅速从1.405Kpa上升到63.204Kpa,挥发损失十分严重,并且会造成尾气排出管堵塞。因此为获得更高的电导率,同时减小挥发损失,避免堵塞,反应温度最高只宜控制在550℃左右。[page]
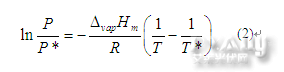
P*:沸点时的蒸汽压即标准大气压 (单位Pa)
P :某一温度下的蒸汽压(单位PaΔ)
ΔvapHm:该物质的摩尔气化热 (单位KJ/mol)
R: 8.314 气体常数(单位KPa m3/kgomolo k)
Zn 的ΔvapHm为114KJ/mol,沸点为907℃,不考虑温度变化对ΔvapHm的影响。
电解产物
在550℃,80A/dm2条件下电解ZnCl2熔盐12h,冷却后发现Zn与ZnCl2固体形成清晰的分层界面(如图6),白色为未电解完的ZnCl2,银色为电解产物Zn。将Zn分离、清洗并干燥,经电感耦合等离子光谱发生仪(ICP)检测,其主要成分为Zn,占70.74%,另外还有Pb(8.451%)、Ni(2.032%)、Fe(0.8013%)等杂质。结果表明利用上述方法电解ZnCl2可成功分离出Zn,其中的杂质主要是ZnCl2原料以及电极棒中的杂质引起,如果直接电解高纯的Zn(99.9999%以上)与高纯的SiCl4(99.9999%以上)反应生成的高纯ZnCl2,电解产物Zn的纯度可达99.99%以上,再经过Zn精馏即可满足Zn还原SiCl4制多晶硅的原料要求。

[page]
结论
针对Zn还原法制多晶硅副产物ZnCl2的回收利用,本文研制了一套小型ZnCl2熔盐电解实验装置,在不添加其他辅助电解质情况下,经初步工艺实验,成功利用ZnCl2熔盐制备出了Zn,纯度可达70.74%,从而验证了ZnCl2电解回收制锌的工艺可行性,并发现反应温度不宜超过550℃。但本文后续研究还有很多工作要做,如采用何种方式准确得到电流效率和单位电能消耗,并以此为基础评价电流密度对电流效率,锌杂质成分、电解温度等的影响等。
另外,本文在实验设备研制和工艺过程中还发现此工艺如向产业化方向推广,还存着以下几个难点:
(1)电解槽材料技术难点
电解槽的使用温度在500℃~600℃之间,内部含有ZnCl2熔盐、Zn液体、Cl2等介质。这样的环境下,金属类材质很容易被腐蚀,不适用。而陶瓷类材料,不易加工成大尺寸。实验阶段,项目组最终选择石英做为电解槽材质。但研究发现,石英电解槽同样也会被ZnCl2缓慢腐蚀,不宜长期使用。而且石英材料易碎,高温下不易密封,做实验设备的材料可以,但不适用于产业化设备。
(2)ZnCl2的电导率过小
ZnCl2的电导率在熔点时仅为0.0024Ω-1ocm-1 ,单独电解槽电压高和能耗相对较大,只有当电极间距很小(10mm以下)时才能有效降低能耗。但在此电极间距下,阴极生成的Zn易与阳极生的Cl2进行二次反应。
(3)液面检测技术难点
由于电解槽温度过高(500℃~600℃),电解槽内部介质的强腐蚀性,传统的液位计不适用于ZnCl2电解槽。生成的Zn液由于比重大落于电解槽底部,Zn的液面目前更没有合适的方法进行检测,目前只能根据理论计算量和经验来判断各液面,并决定电解的中止。